2025年11月3日,Chinese Academy of Agricultural Sciences郑州果树研究所桃遗传育种团队在Horticulture Research(IF = 8.5)上发表了一篇题为“JAZ2/JAZ4-MYC2.1 Module Mediates MeJA-Induced Alleviation of Chilling Injury in Peach Fruit (Prunus persica)"的研究论文。该文章借助DAP-seq技术,揭示了JAZ2/JAZ4-MYC2.1模块介导MeJA缓解桃果实冷害的分子机制。蓝景科信为该研究提供了DAP-seq技术支持。

桃(Prunus persica)作为典型的跃变型果实,因风味佳、营养丰富占据重要市场地位,但采后冷藏易引发冷害(CI),表现为表面凹陷、内部褐变(IB)、成熟受阻等症状,其中内部褐变主要由酚类物质的酶促氧化导致,严重降低果实商品性。茉莉酸甲酯(MeJA)作为植物信号分子,已被证实可增强多种果实的耐冷性,其作用与乙烯合成、抗氧化能力提升等生理过程相关,但MeJA介导桃果实耐冷性的分子机制,尤其是关键转录因子MYC2的调控网络及JAZ蛋白的调控作用,尚未明确。
主要研究结果
核心发现一:生理层面验证MeJA耐冷功效
采用1 mM MeJA浸泡处理‘CP9’桃果实15 min,4℃冷藏28天并系统检测冷害症状及生理指标。结果表明,MeJA处理显著抑制果实内部褐变(IB)发展,显著提高乙烯释放量,同时促进茉莉酸(JA)和JA-Ile积累;果实中总酚、类黄酮等抗氧化物质含量显著升高,丙二醛(MDA)、活性氧(ROS)积累速率及多酚氧化酶(PPO)、过氧化物酶(POD)活性显著降低,有效缓解低温诱导的氧化损伤和组织劣变。

图1 外源茉莉酸甲酯(MeJA)处理缓解桃果实冷害(CI)症状
核心发现二:基因组水平解析核心转录因子PpMYC2.1调控桃果实耐冷三重响应通路
1、锁定PpMYC2.1为耐冷核心调控因子
通过对MeJA处理组和对照组不同冷藏时间的果实进行RNA-seq分析,鉴定差异表达基因(DEGs),并结合系统发育分析、组织特异性表达谱检测。结果发现,两个MYC2(茉莉酸信号分子开关)同源基因中,仅PpMYC2.1在MeJA处理和冷藏期间被持续显著诱导,且其表达量与乙烯合成、多酚和类黄酮积累呈正相关,而PpMYC2.2表达量低且呈负相关。免疫印迹分析证实,MeJA处理可诱导PpMYC2.1蛋白积累,且亚细胞定位显示PpMYC2.1定位在细胞核。以上结果表明,PpMYC2.1是MeJA诱导桃果实耐冷性的重要调控因子,通过整合调控乙烯信号通路和抗氧化物质合成发挥作用。
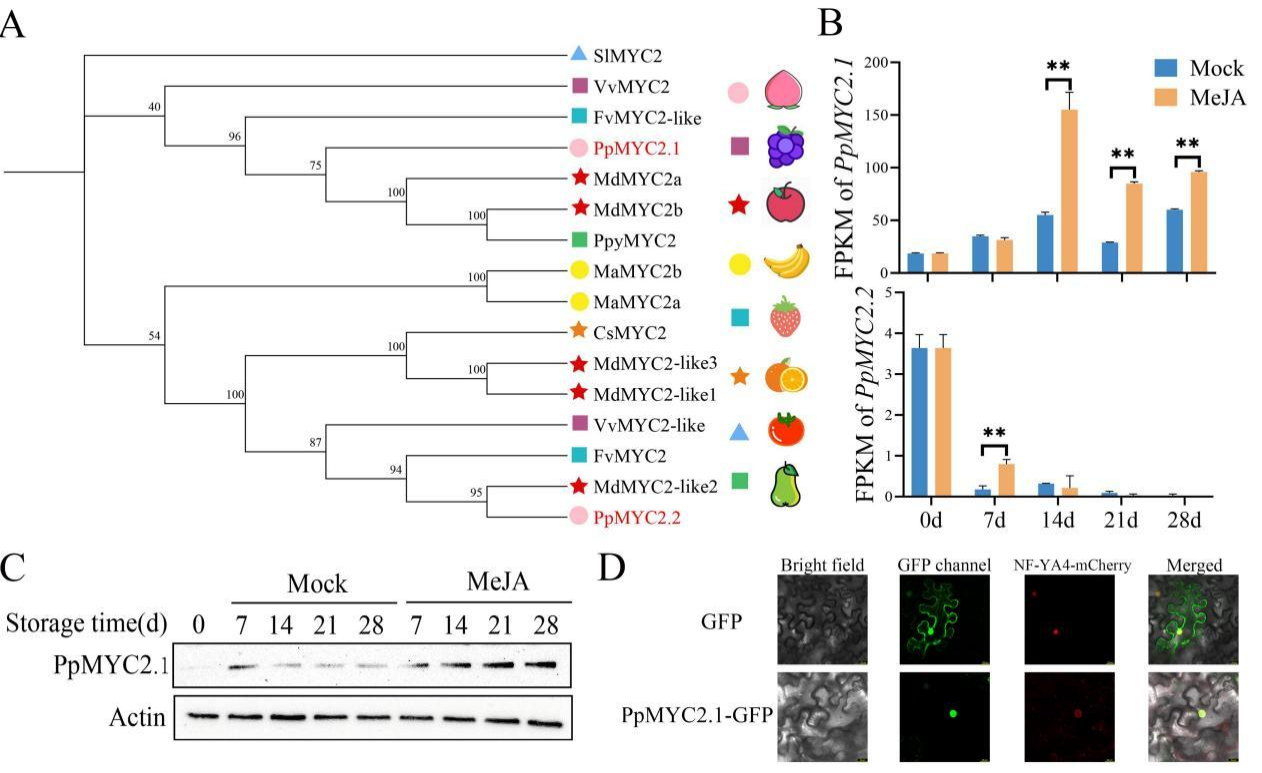
图2 PpMYC2.1在茉莉酸甲酯(MeJA)介导的桃果实茉莉酸(JA)信号通路中发挥作用
2、全基因组鉴定PpMYC2.1靶基因
为鉴定PpMYC2.1的靶基因,研究开展了DNA亲和纯化测序(DAP-seq)。结果显示,PpMYC2.1在桃基因组中存在9752个高置信度结合峰,主要富集于转录起始位点(TSS)上游1000bp区域,其结合基序为CAC[G/A]TG,与经典G-box基序高度相似。进一步结合RNA-seq数据分析,获得1920个PpMYC2.1直接靶基因;GO富集分析显示,这些基因显著富集于苯丙烷生物合成过程、JA介导的信号通路、乙烯响应及细胞壁大分子分解代谢过程,涉及乙烯合成、细胞壁降解和苯丙烷代谢等关键通路。
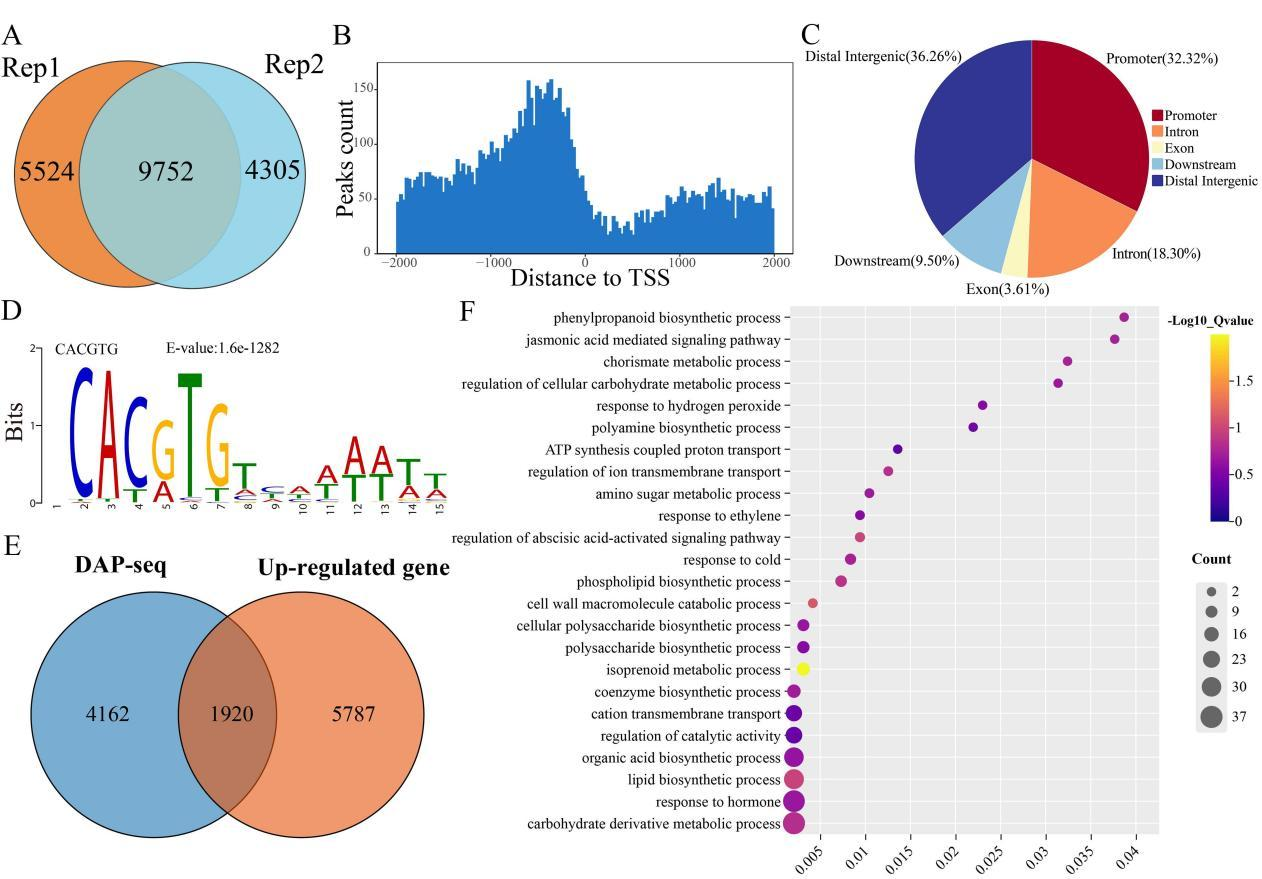
图3 DAP-seq与RNA-seq数据联合分析鉴定到受PpMYC2.1调控的直接靶基因
3、PpMYC2.1调控三大耐冷关键通路
通过DAP-seq和RNA-seq联合分析,筛选出乙烯信号通路关键转录因子(PpIAA1、PpERF61、PpHB.G7)、细胞壁降解相关基因(PpPL1、PpPG2、PpXTH2)以及苯丙烷代谢途径关键基因(PpPAL1、Pp4CL、PpCHI3、PpCHS)。通过Y1H、EMSA、DLR及桃果实瞬时过表达和沉默实验证实,PpMYC2.1可直接结合上述基因的启动子区域并调控其表达,表明PpMYC2.1在介导MeJA诱导的桃果实耐冷性中发挥核心作用。

图4 PpMYC2.1介导的桃果实乙烯合成相关关键转录因子(TFs)的直接调控

图5 PpMYC2.1介导的桃果实细胞壁降解关键基因的直接调控

图6 PpMYC2.1介导的桃果实多酚和类黄酮合成关键基因的直接调控
核心发现三:PpJAZ2/4-MYC2.1模块调控机制与PpMYC2.1耐冷功能的多维验证
1、PpJAZ2/4-PpMYC2.1模块在介导MeJA诱导的桃果实冷适应中的功能
JAZ-MYC模块是JA信号通路中的核心调控机制,其中JAZ蛋白作为抑制因子,通过直接结合并抑制MYC转录因子(TFs)的活性,进而调控下游基因表达。通过系统筛选桃基因组JAZ家族基因,结合转录组分析、蛋白水平检测锁定PpJAZ2/4为候选调控因子。利用酵母双杂交(Y2H)、荧光素酶互补成像(LCI)、双分子荧光互补(BiFC)及免疫共沉淀(Co-IP)等实验证实,PpJAZ2/4与PpMYC2.1存在直接物理相互作用,且二者均定位于细胞核;双荧光素酶报告基因(DLR)实验进一步表明,PpJAZ2/4可显著抑制PpMYC2.1对下游靶基因启动子的激活活性,而MeJA处理能显著下调PpJAZ2/4的转录与蛋白水平,解除其对PpMYC2.1的抑制效应。
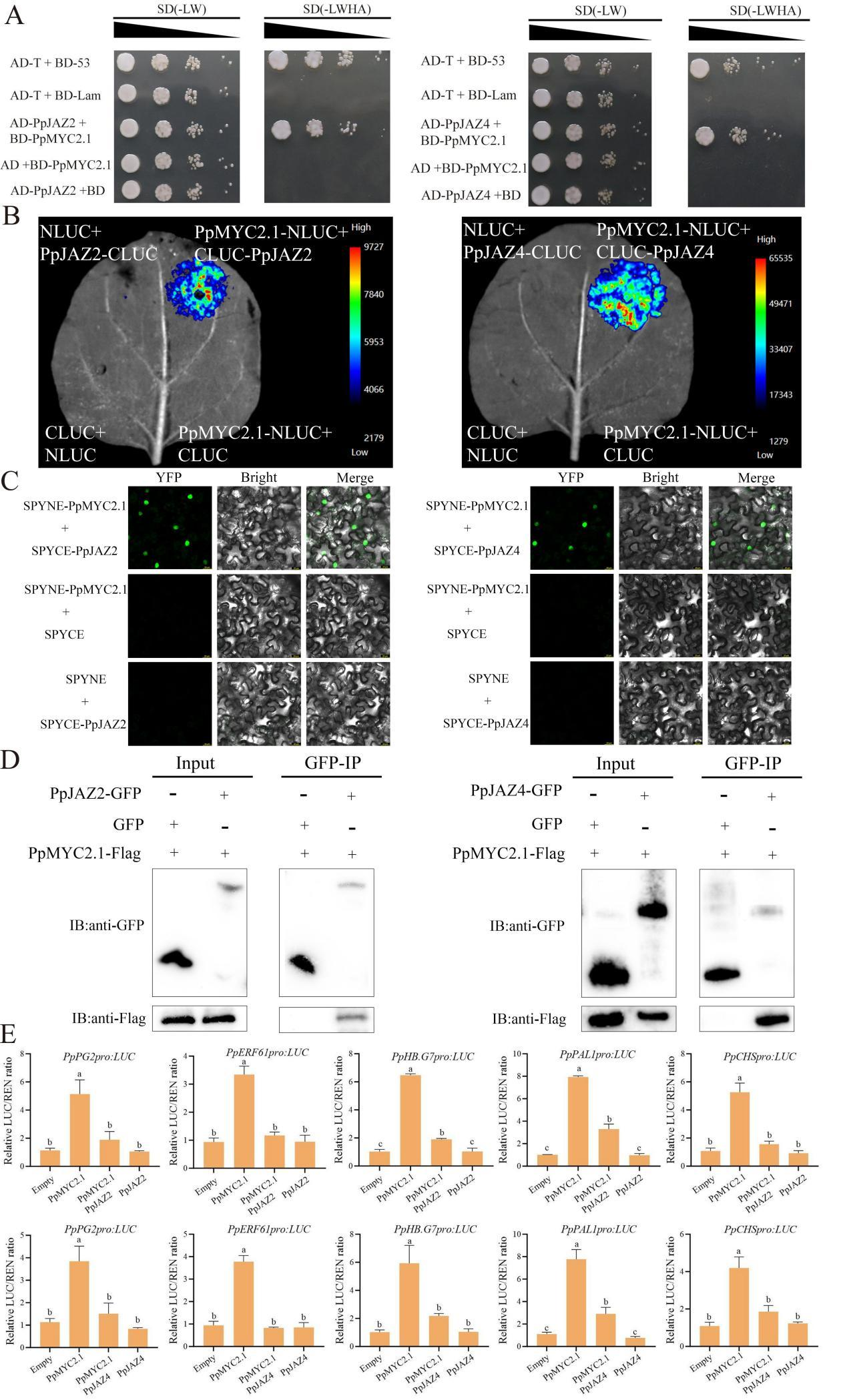
图7 PpJAZ2/4抑制PpMYC2.1对其下游靶基因的转录活性
2、PpMYC2.1跨物种功能验证
为验证PpMYC2.1在调控冷害中的功能作用,本研究构建PpMYC2.1过表达转基因番茄,株系,并对野生型和转基因番茄果实进行4℃冷藏28天处理,检测冷害症状及相关理化和分子指标。结果显示,转基因番茄冷害指数显著低于WT,乙烯合成量显著提升,果实硬度适度下降,MDA和ROS积累减少,总酚、类黄酮含量升高,且乙烯合成(SlACS2、SlACO1)、细胞壁降解(SlPL1、SlXTH3)及苯丙烷代谢(SlPAL1、SlCHS1)相关基因转录水平显著上调。以上结果表明,PpMYC2.1的耐冷功能在不同果实物种中具有保守性。

图8 转基因番茄果实中PpMYC2.1过表达增强耐冷性
小结
本研究通过多组学技术(RNA-seq、DAP-seq)与分子生物学实验相结合,完整揭示了“MeJA下调PpJAZ2/4表达→解除对PpMYC2.1的抑制→激活乙烯合成、细胞壁重塑及多酚类黄酮合成通路→增强果实耐冷性"的分子调控链。这一发现不仅填补MeJA介导桃果实耐冷害分子机制的研究空白,更为跃变型果实采后冷链物流优化提供了关键分子靶点,为开发高效、绿色的保鲜技术奠定了坚实的理论基础。

图9 阐明PpMYC2.1在提升耐冷性中正向调控作用的工作模型
