
文献题目:ONAC122 and ONAC131, controlled by OsSRWD1, OsRACK1A, and OsRGLG2, regulate rice immunity through modulating OsRFPH2-2 and OsBIERF3
发表期刊:New Phytologist
影响因子:8.1
物种:水稻
作者单位:浙江大学
发表时间:2026年2月24日
蓝景科信提供:DAP-seq技术服务
主要研究结果
植物先天免疫系统是其抵御病原菌侵染的核心防线,主要包括病原/微生物/损伤相关分子模式触发的免疫(PTI)和效应因子触发的免疫(ETI)两大层面。二者通过启动复杂的信号级联反应,激活NAC、WRKY、ERF等多个家族的转录因子(TFs),驱动免疫相关基因的转录重编程,最终实现对病原菌的抗性响应。稻瘟病由稻瘟病菌(Magnaporthe oryzae)引起,是水稻生产中破坏性的真菌病害之一,严重威胁全球粮食安全。解析水稻抗稻瘟病的分子调控网络,挖掘关键抗病基因,是培育抗病水稻品种的核心基础。
NAC转录因子是植物的核心转录因子家族,其N端为保守DNA结合域,C端为转录调控可变域,在生长发育与逆境应答中至关重要。水稻151个NAC成员中已有21个被证实参与免疫调控,其中ONAC122和ONAC131可正向调控稻瘟病抗性,但其作用机制、靶基因、上游调控及结合元件等关键科学问题仍未阐明。
该研究利用RNA-seq比较onac122、onac131突变体、过表达株系与野生型的转录组差异,GO与KEGG富集分析表明,相关差异表达基因主要富集在植物-病原菌互作、MAPK 信号通路等免疫相关通路。进一步通过DAP-seq鉴定ONAC122全基因组结合位点,其中24.6%富集于基因启动子区,且其核心结合顺式作用元件为经典的CACG,同时鉴定出其可结合的新型ACTC元件。随后通过酵母双杂交、双分子荧光互补及免疫共沉淀实验证实,ONAC122与ONAC131可形成同源及异源二聚体,ONAC131不直接激活靶基因,但可协同增强ONAC122对OsRFPH2-2和OsBIERF3的转录激活。而OsSRWD1和OsRACK1A作为互作蛋白,特异性增强ONAC122的转录活性,正向调控该模块的免疫功能;而具有E3泛素连接酶活性的OsRGLG2,则通过泛素化修饰并经26S蛋白酶体途径降解ONAC122和ONAC131,抑制其功能,进而负调控水稻对稻瘟病的抗性。
该研究不仅为水稻抗稻瘟病的分子机制研究奠定了重要基础,也为植物先天免疫系统的调控研究提供了新的视角,其研究成果兼具理论价值和应用价值,对保障水稻生产安全、推动植物抗病分子育种发展具有重要意义。
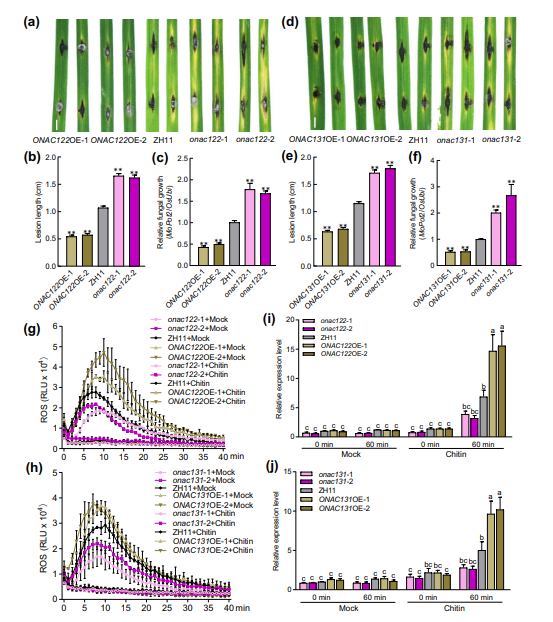
图1. ONAC122和ONAC131在水稻稻瘟病抗性及几丁质触发的病原相关分子模式诱导免疫(PTI)中的正调控作用。(a~f)ONAC122(a~c)和ONAC131(d~f)正向调控水稻的稻瘟病抗性。采用打孔接种法,向onac122突变体、ONAC122过表达株系、onac131突变体、ONAC131过表达株系及ZH11的代表性叶片接种10 uL稻瘟病菌RB22菌株的孢子悬浮液(浓度为5×10⁵个・mL-1)后,观察叶片的病害症状(a、d)、测定病斑长度(b、e)并检测稻瘟病菌在植株体内的相对生物量(c、f)。在接种后第5天记录病害表型并采集叶片样品(比例尺=0.2 cm)。采用荧光定量PCR法对病菌相对生物量进行定量分析,以稻瘟病菌MoPot2基因的表达量相对于水稻泛素基因OsUbi的表达量的倍数表示。图b、c、e、f中数据以平均值±标准误表示,其中b、e的样本量n=27,c、f的样本量n=9。(g、h)几丁质处理后,onac122突变体、ONAC122过表达株系(g)以及onac131突变体、ONAC131过表达株系(h)中的活性氧(ROS)爆发情况。(i、j)几丁质处理后,onac122突变体、ONAC122过表达株系(i)以及onac131突变体、ONAC131过表达株系(j)和ZH11植株中OsWRKY45基因的表达变化。将水稻叶圆片在水中过夜预培养后,用浓度为100ug・mL-1的几丁质处理,以清水处理作为阴性对照;立即检测化学发光信号,以相对光单位(RLU)表示检测结果(g、h)。在处理后指定时间点采集叶片样品,进行基因表达分析,以水稻18SrRNA基因为内参对数据进行标准化处理(i、j)。图g、h中数据以平均值±标准误表示,样本量n=3;图i、j中样本量n=9。注:b、c、e、f中**表示与ZH11相比,差异极显著(P<0.01,Student's t检验);i、j中不同字母表示组间差异显著(P<0.05,单因素方差分析)。所有实验均独立重复3次,结果一致。
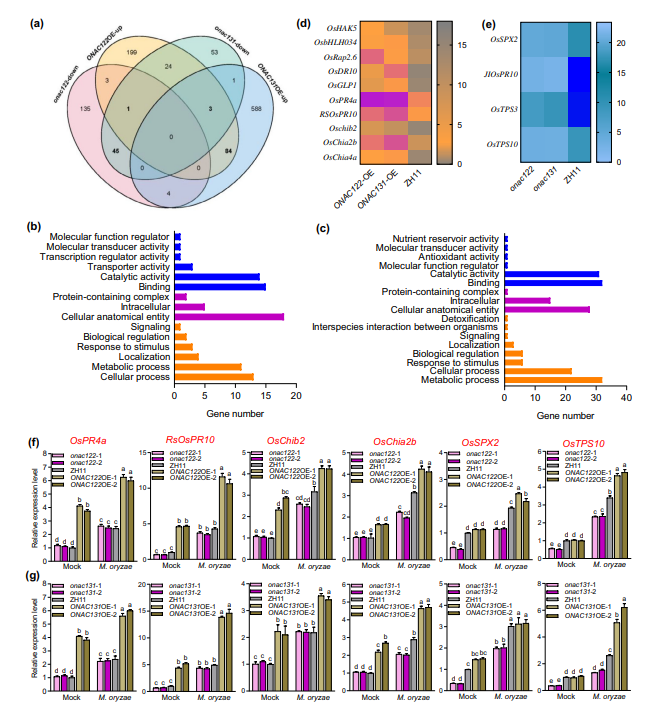
图2. 转录组测序分析水稻onac122突变体、ONAC122过表达株系、onac131突变体及ONAC131过表达株系中的差异表达基因。(a)韦恩图展示未接稻瘟病菌时,与ZH11相比,在onac122和onac131突变体中下调、且在ONAC122和ONAC131过表达株系中上调的差异表达基因分布情况。(b、c)与ZH11相比,ONAC122和ONAC131过表达株系中上调基因(b)、onac122和onac131突变体中下调基因(c)的GO功能富集分析结果。(d、e)与ZH11相比,ONAC122和ONAC131过表达株系(d)、onac122和onac131突变体(e)中免疫相关基因的表达变化。(f、g)经稻瘟病菌接种或未接种处理后,onac122突变体、ONAC122过表达株系(f),以及onac131突变体、ONAC131过表达株系(g)和ZH11中筛选出的免疫相关基因的表达模式。对三周龄水稻植株采用叶面喷雾法接种稻瘟病菌RB22菌株的孢子悬浮液(浓度为2×10⁵个・mL-1),并以0.05%的吐温-20喷雾处理作为空白对照;在接种后指定时间点采集叶片样品进行基因表达分析,以水稻18SrRNA基因为内参对数据进行标准化处理。图f、g中数据以平均值±标准误表示,样本量n=3;不同字母表示组间差异达到显著水平(P<0.05,单因素方差分析)。所有实验均独立重复3次,实验结果一致。
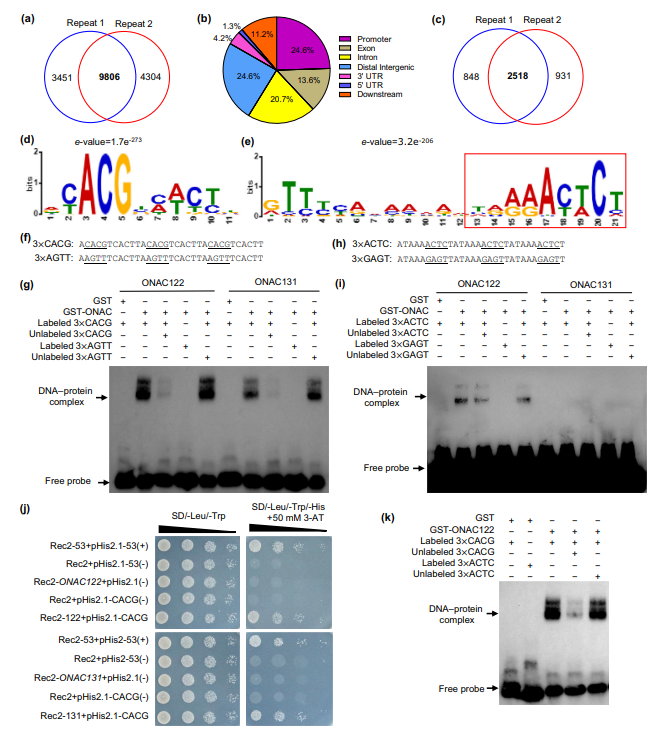
图3. 水稻ONAC122的全基因组结合位点及ONAC122、ONAC131对CACG和ACTC顺式作用元件的结合活性。(a)经DAP-seq分析得到的两个生物学重复中,ONAC122高可信度结合峰的统计结果。(b)DAP-seq分析鉴定的ONAC122结合峰在基因区域及染色体其他区域的分布情况。(c)两个生物学重复的DAP-seq分析中,ONAC122在基因启动子区的高可信度结合峰统计结果。(d、e)被鉴定为ONAC122结合序列的CACG元件(d)和ACTC元件(e)。(f~i)电泳迁移率变动实验(EMSA)中,ONAC122、ONAC131对CACG元件(f、g)、ACTC元件(h、i)及其突变体的结合活性。将Bio标记的探针,与GST-ONAC122蛋白、GST-ONAC131蛋白或纯化的GST蛋白(作为阴性对照)共孵育,设置添加或不添加过量(20倍)非标记探针的实验组。特异性DNA-蛋白复合物与游离探针均用黑色箭头标注。(j)酵母单杂交实验(Y1H)中,ONAC122、ONAC131对CACG顺式作用元件的结合活性。将转入指定Rec2载体与pHis2载体组合的酵母细胞,经梯度稀释后,分别培养在SD/缺Trp/缺Leu、SD/缺Trp/缺Leu/缺His+30mmol/L3-氨基-1,2,4-三唑(3-AT)、SD/缺Trp/缺Leu/缺His+50mmol/L3-AT培养基上。(k)ACTC识别序列无法与CACG识别序列竞争结合ONAC122。将Bio标记的3×CACG探针,与GST-ONAC122蛋白或纯化的GST蛋白(作为阴性对照)共孵育,设置添加或不添加过量(20倍)非标记3×ACTC探针的实验组。特异性DNA-蛋白复合物与游离探针均用黑色箭头标注。所有实验均独立重复3次,实验结果一致。
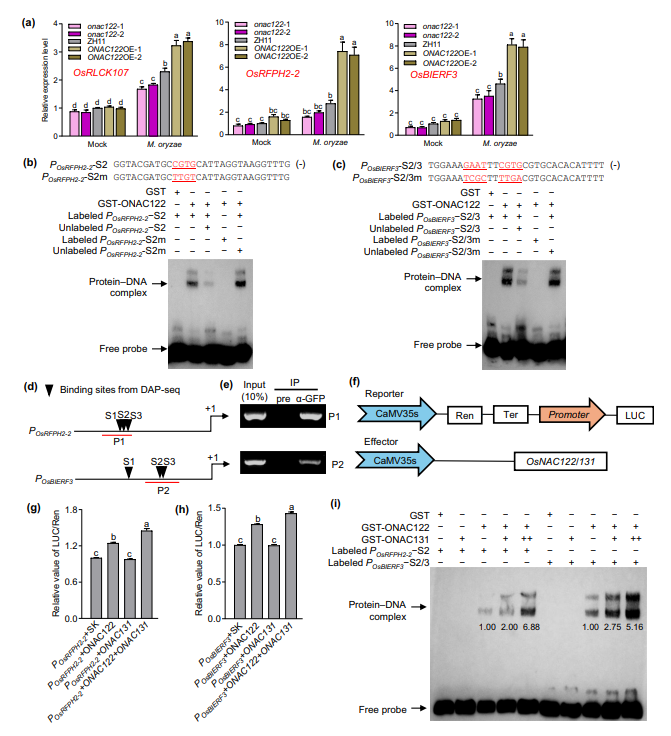
图4. 水稻ONAC122对OsRFPH2-2和OsBIERF3启动子的结合活性及其对二者的转录激活作用。(a) 稻瘟病菌接种与未接种条件下,onac122突变体和ONAC122过表达株系中OsRLCK107、OsRFPH2-2和OsBIERF3 基因的相对表达量。对三周龄水稻植株采用叶面喷雾法,接种稻瘟病菌RB22菌株的孢子悬浮液(浓度为2×10⁵个・mL-1),并以0.05%吐温-20喷雾处理作为空白对照;在接种后指定时间点采集叶片样品进行基因表达分析,以水稻18SrRNA基因为内参完成数据标准化。实验数据以平均值±标准误表示,样本量n=9。(b、c)电泳迁移率变动实验验证ONAC122与OsRFPH2-2启动子S2位点(b)、OsBIERF3启动子S2/S3位点(c)中CACG顺式作用元件的结合作用。图中CACG元件以红色字体标注并添加下划线,(+)表示正链,(-)表示负链。将含CACG顺式作用元件的30bp片段及其突变体片段进行Bio标记,与GST-ONAC122蛋白共孵育,同时设置添加/不添加20倍过量非标记探针的实验组,以纯化的GST蛋白作为阴性对照。特异性DNA-蛋白复合物与游离探针均用黑色箭头标注。(d)经DAP-seq鉴定的OsRFPH2-2和OsBIERF3启动子中潜在的CACG顺式作用元件位点。其中P1和P2为ChIP-PCR所用探针,S1、S2、S3为启动子区域的CACG顺式作用元件位点。(e)ChIP-PCR实验验证ONAC122在体内与OsRFPH2-2和OsBIERF3启动子片段的结合作用。提取ONAC122-GFP融合蛋白表达株系的染色质片段化DNA,与GFP抗体(α-GFP)共孵育,以免疫前血清(Pre)作为阴性对照;将免疫沉淀(IP)样品、免疫沉淀前的染色质DNA(阳性对照/输入样品)用于PCR扩增检测。(f)双荧光素酶报告基因实验中所用的ONAC122、ONAC131效应载体及靶基因启动子报告载体示意图。(g、h)本氏烟草叶片中瞬时共表达ONAC122和/或ONAC131与OsRFPH2-2(g)、OsBIERF3(h)启动子后的相对荧光素酶/海肾荧光素酶(LUC/Ren)活性值。实验数据以平均值±标准误表示,样本量n=6。(i)ONAC131可提高ONAC122对含CACG元件的OsRFPH2-2和OsBIERF3启动子片段的结合亲和力。将Bio标记的探针与重组GST-ONAC122蛋白单独孵育,或与GST-ONAC122和GST-ONAC131蛋白共同孵育;特异性DNA-蛋白复合物与游离探针用黑色箭头标注,蛋白相对表达量采用IMAGEJ软件进行定量分析。注:a、g、h中不同字母表示组间差异达到显著水平(P<0.05,单因素方差分析);所有实验均至少独立重复3次,结果一致。
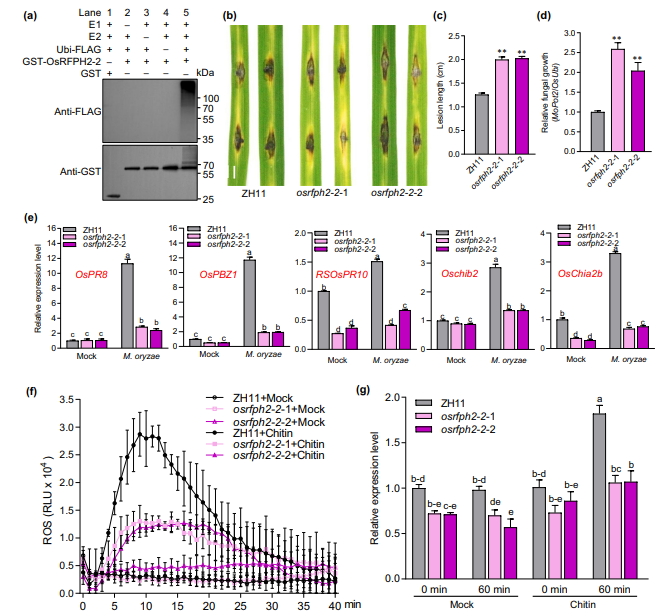
图5. OsRFPH2-2 在水稻稻瘟病抗性及几丁质触发的模式触发免疫(PTI)中的正调控作用。(a)OsRFPH2-2的E3泛素连接酶活性检测。将GST融合OsRFPH2-2蛋白与人类E1、E2泛素结合酶及FLAG标签泛素在30℃条件下共孵育3小时,采用抗GST抗体和抗FLAG抗体分别检测蛋白泛素化修饰水平与蛋白表达量。(b~d)OsRFPH2-2基因敲除突变体的稻瘟病抗性显著降低。采用打孔接种法,向代表性的osrfph2-2突变体和ZH11叶片接种10 uL稻瘟病菌RB22菌株的孢子悬浮液(浓度为5×10⁵个・mL-1),观察叶片的病害症状(b)、测定病斑长度(c)并检测病菌在植株体内的相对生物量(d)。在接种后第5天记录病害表型并采集叶片样品,比例尺为0.2 cm。采用荧光定量PCR法检测病菌相对生物量,以稻瘟病菌MoPot2基因表达量相对于水稻泛素基因OsUbi的倍数表示。实验数据以平均值±标准误表示,其中c的样本量n=27,d的样本量n=9。(e)稻瘟病菌接种与未接种条件下,osrfph2-2突变体和ZH11中抗病相关基因的表达变化。对三周龄水稻植株采用叶面喷雾法接种稻瘟病菌RB22菌株的孢子悬浮液(浓度为2×10⁵个・mL-1),并以等体积0.05%吐温-20溶液喷雾处理作为阴性对照;在接种后48小时采集叶片样品进行基因表达分析,以水稻18SrRNA基因为内参完成数据标准化。实验数据以平均值±标准误表示,样本量n=9。(f、g)osrfph2-2突变体和ZH11中几丁质触发的活性氧(ROS)爆发情况(f)及OsWRKY45基因的表达变化(g)。将水稻叶圆片在清水中过夜预培养后,用浓度为100 ug・mL-1的几丁质处理,以清水处理作为阴性对照;立即检测化学发光信号,结果以相对光单位(RLU)表示(f)。在处理后指定时间点采集叶片样品进行基因表达分析,以水稻18SrRNA基因为内参完成数据标准化(g)。实验数据以平均值±标准误表示,其中f的样本量n=3,g的样本量n=9。注:c、d中**表示与ZH11相比差异极显著(P<0.01,Student's t检验);e、g中不同字母表示组间差异显著(P<0.05,单因素方差分析)。所有实验均至少独立重复3次,结果一致。
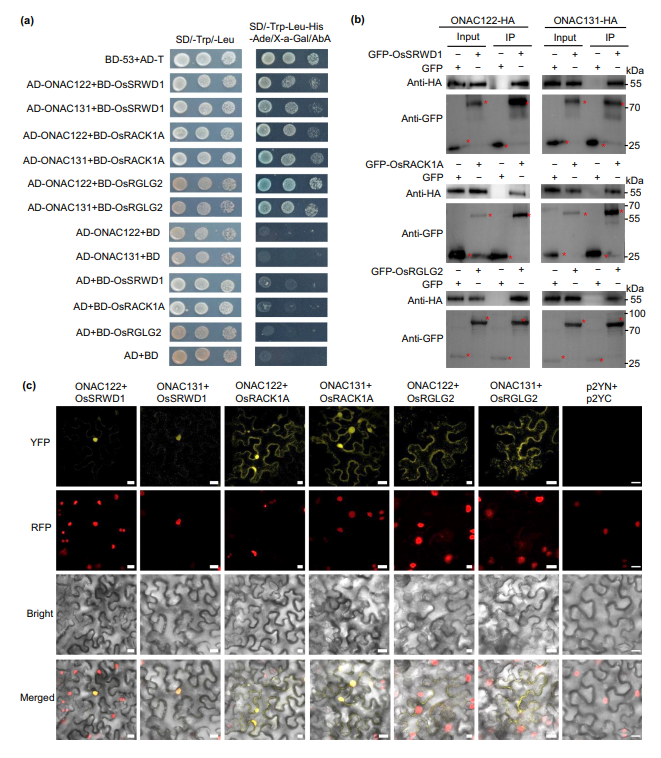
图6. 水稻 ONAC122、ONAC131 与 OsSRWD1、OsRACK1A 及 OsRGLG2 的蛋白互作关系。(a)酵母双杂交(Y2H)实验验证ONAC122、ONAC131与OsSRWD1、OsRACK1A、OsRGLG2的互作。将含有指定重组pGBKT7载体与pGADT7载体组合的酵母菌株,分别培养在SD/缺Trp/缺Leu培养基或SD/缺Trp/缺Leu/缺His/缺腺嘌呤/5-溴-4-氯-3-吲哚-β-D-半乳糖苷(X-α-gal)/金担子素A(AbA)培养基上,根据酵母菌落的生长情况判断蛋白间是否存在互作。(b)免疫共沉淀(Co-IP)实验验证ONAC122、ONAC131与OsSRWD1、OsRACK1A、OsRGLG2的互作。将携带重组pCAMBIA1300-GFP载体、pFGC1008-HA载体或空pCAMBIA1300-GFP载体的农杆菌,按指定组合共浸润至本氏烟草叶片中;浸润后48小时提取总蛋白,用GFP亲和磁珠进行3小时免疫沉淀,随后分别采用抗GFP抗体和抗HA抗体进行免疫印迹检测,目标蛋白用红色星号标注。(c)双分子荧光互补(BiFC)实验验证ONAC122、ONAC131与OsSRWD1、OsRACK1A、OsRGLG2的互作。将携带重组或空p2YN载体与p2YC载体的农杆菌,分别共浸润至表达核定位标记蛋白RFP-H2B的本氏烟草叶片中;浸润后48小时观察荧光信号,比例尺为20 um。所有实验均独立重复3次,结果一致。
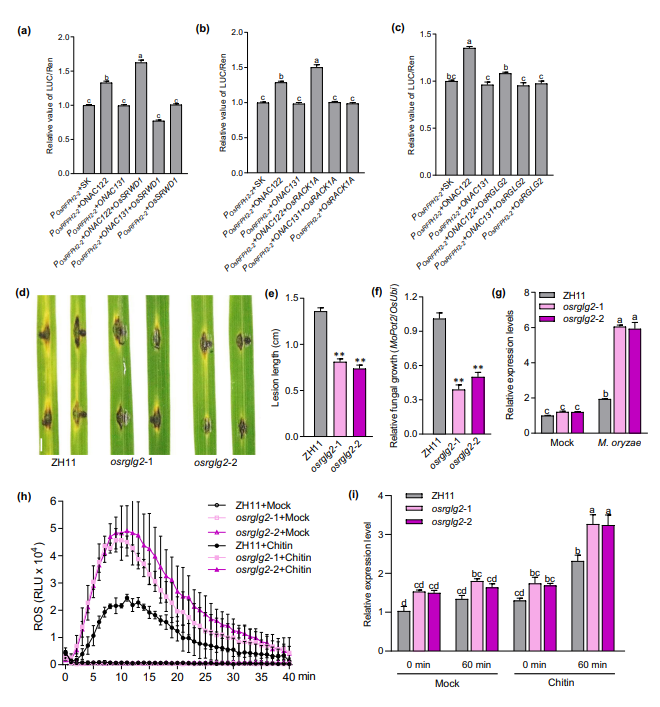
图7. OsSRWD1、OsRACK1A及OsRGLG2对ONAC122转录活性的影响,以及 OsRGLG2 在水稻稻瘟病抗性和几丁质触发的模式触发免疫(PTI)中的负调控作用。(a~c)在OsRFPH2-2启动子存在的条件下,本氏烟草叶片中瞬时共表达ONAC122、ONAC131与OsSRWD1(a)、OsRACK1A(b)或OsRGLG2(c)后的相对荧光素酶/海肾荧光素酶(LUC/Ren)活性值。实验数据以平均值±标准误表示,样本量n=6。(d~f)OsRGLG2基因敲除突变体(osrglg2)的稻瘟病抗性显著增强。采用打孔接种法,向代表性的osrglg2突变体和ZH11叶片接种10 uL稻瘟病菌RB22菌株的孢子悬浮液(浓度为5×10⁵个・mL-1),观察叶片的病害症状(d)、测定病斑长度(e)并检测病菌在植株体内的相对生物量(f)。在接种后第5天记录病害表型并采集叶片样品,比例尺为0.2 cm。采用荧光定量PCR法检测病菌相对生物量,以稻瘟病菌MoPot2基因表达量相对于水稻泛素基因OsUbi的倍数表示。实验数据以平均值±标准误表示,其中e的样本量n=27,f的样本量n=9。(g)稻瘟病菌接种与未接种条件下,osrglg2突变体和ZH11中OsPBZ1基因的表达变化。对三周龄水稻植株采用叶面喷雾法接种稻瘟病菌RB22菌株的孢子悬浮液(浓度为2×10⁵个・mL-1),并以等体积0.05%吐温-20喷雾处理作为阴性对照;在接种后48小时采集叶片样品进行基因表达分析,以水稻18SrRNA基因为内参完成数据标准化。实验数据以平均值±标准误表示,样本量n=9。(h、i)osrglg2突变体和ZH11中几丁质触发的活性氧(ROS)爆发情况(h)及OsWRKY45基因的表达变化(i)。将水稻叶圆片在清水中过夜预培养后,用浓度为100 μg・mL-1的几丁质处理,以清水处理作为阴性对照;立即检测化学发光信号,结果以相对光单位(RLU)表示(h)。在处理后指定时间点采集叶片样品进行基因表达分析,以水稻18SrRNA基因为内参完成数据标准化(i)。实验数据以平均值±标准误表示,其中h的样本量n=3,i的样本量n=9。注:a~c、g、i中不同字母表示组间差异显著(P<0.05,单因素方差分析);e、f中**表示与ZH11相比差异极显著(P<0.01,Student'st检验)。所有实验均独立重复3次,结果一致。
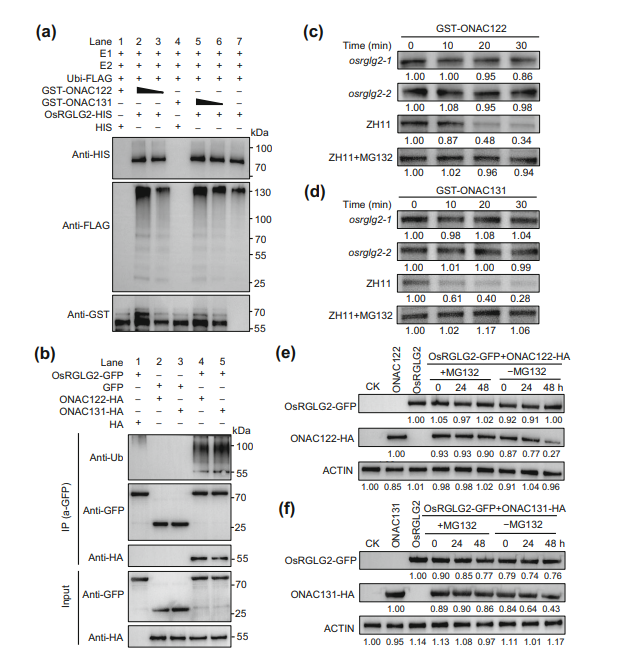
图8. 水稻中OsRGLG2介导的ONAC122和ONAC131泛素化修饰与降解。(a)OsRGLG2的E3泛素连接酶活性及体外对ONAC122、ONAC131的泛素化修饰。将OsRGLG2-HIS与GST-ONAC122或GST-ONAC131,在人类E1、E2泛素结合酶及FLAG标签泛素存在的条件下,于30℃共孵育3小时。采用抗HIS抗体、抗GST抗体及抗FLAG抗体分别检测蛋白泛素化修饰水平与蛋白表达量。(b)本氏烟草叶片中OsRGLG2对ONAC122、ONAC131的泛素化修饰。将携带指定重组载体(pCAMBIA1300-OsRGLG2-GFP、pFGC1008-ONAC122-HA、pFGC1008-ONAC131-HA)或空载体(pCAMBIA1300-GFP、pFGC1008-HA)的农杆菌共浸润至本氏烟草叶片;浸润后48小时提取总蛋白,用GFP亲和磁珠免疫沉淀3小时,随后采用抗HA抗体、抗GFP抗体及抗泛素抗体进行免疫印迹检测。(c、d)无细胞降解实验验证OsRGLG2介导的GST-ONAC122(c)和GST-ONAC131(d)降解。将GST-ONAC122、GST-ONAC131分别与OsRGLG2基因敲除突变体(osrglg2)和ZH11的总蛋白提取物共孵育,设置添加或不添加50μM蛋白酶体抑制剂MG132的实验组,通过抗GST抗体免疫印迹检测目标蛋白的降解情况。(e、f)本氏烟草叶片中OsRGLG2介导的ONAC122(e)和ONAC131(f)降解。将携带指定重组载体(pCAMBIA1300-OsRGLG2-GFP、pFGC1008-ONAC122-HA、pFGC1008-ONAC131-HA)的农杆菌共浸润至本氏烟草叶片,在浸润后24小时添加或不添加50μMMG132;提取总蛋白后,采用抗GFP抗体、抗HA抗体及抗Actin抗体进行免疫印迹检测。所有实验均独立重复3次,结果一致。
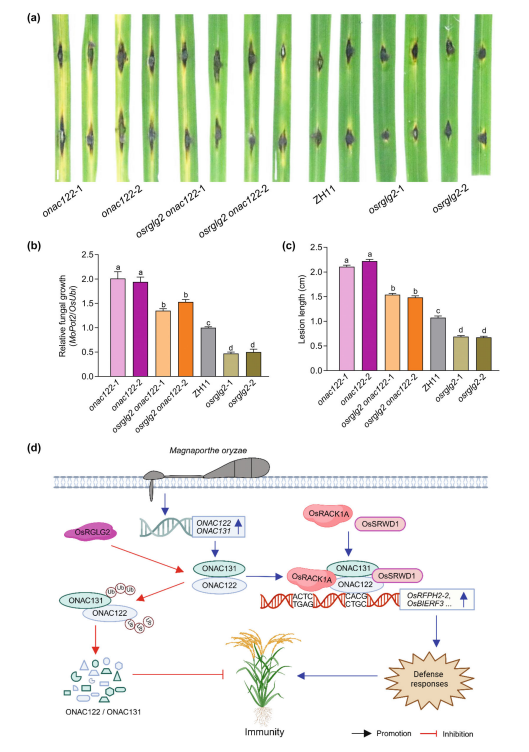
图9. osrglg2 onac122 双突变体稻瘟病抗性减弱及OsRGLG2-ONAC122/131-OsRFPH2-2调控水稻免疫的模式图。(a~c)osrglg2onac122双突变体的稻瘟病抗性显著减弱。采用打孔接种法,向代表性的onac122单突变体、osrglg2单突变体、osrglg2onac122双突变体及ZH11叶片接种10uL稻瘟病菌RB22菌株的孢子悬浮液(浓度为5×10⁵个・mL-1),观察叶片的病害症状(a)、测定病斑长度(b)并检测病菌在植株体内的相对生物量(c)。在接种后第5天记录病害表型并采集叶片样品,比例尺为0.2厘米。采用荧光定量PCR法检测病菌相对生物量,以稻瘟病菌MoPot2基因表达量相对于水稻泛素基因OsUbi的倍数表示。实验数据以平均值±标准误表示,其中b的样本量n=27,c的样本量n=9。b、c中不同字母表示组间差异显著(P<0.05,单因素方差分析)。所有实验均独立重复3次,结果一致。(d)OsRGLG2-ONAC122/131-OsRFPH2-2调控水稻免疫的模式图。NAC转录因子ONAC122可通过转录激活下游靶基因(包括OsRFPH2-2和OsBIERF3)的表达,正向调控水稻免疫;ONAC131可协同增强ONAC122介导的转录激活作用。ONAC122和ONAC131均能与OsSRWD1、OsRACK1A及OsRGLG2发生互作,其中OsSRWD1和OsRACK1A可增强ONAC122的转录活性,而OsRGLG2则抑制其转录活性。具有活性的E3泛素连接酶OsRGLG2可通过泛素化修饰ONAC122和ONAC131并促进二者降解,进而抑制水稻免疫。图中“促进作用"以箭头表示,代表激活或上调;“抑制作用"以钝端箭头表示,代表抑制或下调。该模式图通过BioRender软件绘制。

上一篇 : KEGG富集分析超详细解读
下一篇 : DAP-seq如何成为植物功能基因研究关键技术?